Validasi Metode Pengujian Non Standar Rapid Test Kit di Laboratorium

Validasi non standar rapid test kit ISO 17025 menjadi langkah penting untuk memastikan keakuratan hasil pengujian di laboratorium. Berdasarkan Sistem Manajemen Mutu ISO/IEC 17025 klausul 7.2, dinyatakan bahwa “Laboratorium harus melakukan validasi metode untuk metode non-standar, metode yang dikembangkan sendiri, dan modifikasi metode standar untuk memastikan metode tersebut sesuai dengan penggunaan yang dimaksud.” Proses validasi metode non standar rapid test kit diperlukan pengujian untuk membuktikan bahwa prosedur yang digunakan mampu menghasilkan data yang presisi serta dapat dipercaya.
Dalam beberapa tahun terakhir, rapid test kit semakin banyak digunakan sebagai pilihan alternatif, khususnya untuk kebutuhan pengujian langsung di lapangan (onsite).
Artikel ini akan membahas proses validasi metode non-standar rapid test kit di laboratorium.
Pengujian Rapid Test Kit
Langkah-Langkah Pengujian
Rapid test kit biasanya terdiri dari alat uji cepat, vial, dan reagen kit. Sebagai contoh, pengujian nitrit dengan rapid test kit umumnya meliputi :
- Siapkan 10 mL sampel ke dalam vial pengujian.
- Letakkan vial di alat untuk proses kalibrasi nol.
- Tambahkan larutan reagen, kemudian homogenkan.
- Masukkan kembali vial ke alat, tekan tombol “Test”, lalu tunggu ±10 menit.
- Baca dan dokumentasikan hasil kadar nitrit yang tertera.
Keunggulan Rapid Test Kit
Rapid test kit memiliki sejumlah kelebihan dibandingkan metode analisis konvensional, antara lain :
- Ekonomis dan mudah dioperasikan, bahkan oleh pengguna tanpa keterampilan teknis mendalam.
- Reagen sudah tersedia dalam satu paket, sehingga proses pengujian lapangan menjadi lebih praktis.
- Minim limbah dan penggunaan reagen, sehingga ramah lingkungan dan efisien.
- Hasil uji cepat, dapat diperoleh dalam hitungan menit dan dapat ditelusuri ke sistem satuan internasional.
Perencanaan Validasi Metode
Langkah awal sebelum memvalidasi metode adalah mempertimbangkan berbagai faktor, seperti keterbatasan sumber daya laboratorium, kebutuhan pelanggan, dan aplikasi rutin metode tersebut.
Sebelum memulai validasi, laboratorium perlu mempertimbangkan :
- Ketersediaan sumber daya laboratorium
- Kebutuhan pelanggan
- Aplikasi rutin metode tersebut
Persiapan teknis meliputi:
- Peningkatan kompetensi personel melalui uji kompetensi
- Pemilihan metode sesuai standar nasional atau internasional
- Kalibrasi peralatan
- Penggunaan reagen, CRM, dan air bebas kontaminan sesuai spesifikasi
Parameter Validasi Metode
Evaluasi bias dilakukan dengan membandingkan hasil uji terhadap nilai referensi dari CRM. Presisi diukur dari keberulangan hasil menggunakan %RSD dan %RPD.
1. Penilaian Bias, Ketepatan, dan Presisi
- Bias : dibandingkan dengan nilai referensi dari CRM.
- Presisi : dinilai dari keberulangan hasil (%RSD dan %RPD).
Batas keberterimaan metode:
- %RPD atau %RSD ≤ 10%
- Recovery: 85% – 115%
Jika tidak ada batas keberterimaan khusus, dapat mengacu pada AOAC (tabel disesuaikan seperti di teks asli).
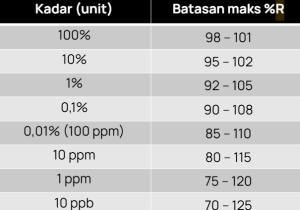
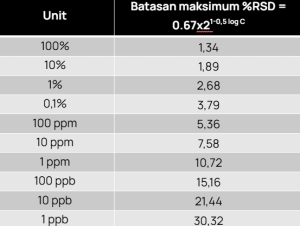
Baca juga validasi metode uji kimia
2. Batas Deteksi (LoD) dan Batas Kuantifikasi (LoQ)
Menetapkan batas deteksi suatu metode menjadi indikator kemampuan dan keterbatasan laboratorium dalam menerapkan metode tersebut untuk menemukan analit pada kadar yang sangat rendah.
Tujuan penetapan batas deteksi adalah memastikan hasil uji tidak hanya disajikan sebagai “tidak terdeteksi” (ND) tanpa nilai acuan, karena hal ini dapat membuat informasi kurang bermakna dan sulit diinterpretasikan tanpa angka batas deteksi minimum.
Proses validasi juga mencakup pengukuran tingkat sensitivitas metode dalam mendeteksi analit pada konsentrasi rendah, dengan mempertimbangkan parameter berikut :
- IDL: sinyal 3–5 kali signal-to-noise dari pengujian larutan blanko.
- LLD/LoD: konsentrasi terkecil yang dapat terdeteksi di atas blanko.
- MDL: peluang deteksi 99% di atas sinyal blanko, dengan minimal 7 ulangan selama 3 hari berbeda.
- LoQ: konsentrasi terendah yang masih dapat diukur secara kuantitatif (perhitungan = 10 × SD).
3. Repeatabilitas & Reprodusibilitas
Dua aspek penting lain yang dievaluasi adalah diantaranya adalah Repeatabilitas dan Reprodusibilitas.
- Repeatabilitas: pengujian dilakukan oleh analis yang sama pada waktu yang sama.
- Reprodusibilitas: pengujian dilakukan oleh analis berbeda atau pada waktu yang berbeda. Penilaian dilakukan pada konsentrasi rendah (0,04 mg/L), sedang (0,39 mg/L), dan tinggi (0,8 mg/L) untuk memastikan stabilitas hasil.
Kesimpulan
Validasi metode berfungsi untuk memastikan bahwa rapid test kit non-standar dapat dipakai di laboratorium dengan menghasilkan data yang akurat dan sesuai standar yang dipersyaratkan. Proses validasi meliputi pengujian presisi, bias, sensitivitas, hingga ketepatan pengulangan. Dengan validasi yang tepat, rapid test kit dapat menjadi solusi cepat, praktis, dan terpercaya dalam pengujian laboratorium.
Cari panduan praktis validasi rapid test kit agar hasil pengujian lebih terjamin? Hubungi melalui bit.ly/tanyalichemindo

Baca juga artikel Memahami GLP dan ISO 17025




